Kostenlose Vorlage zum Download
- Kostenloser Download
- Direkt verfügbar
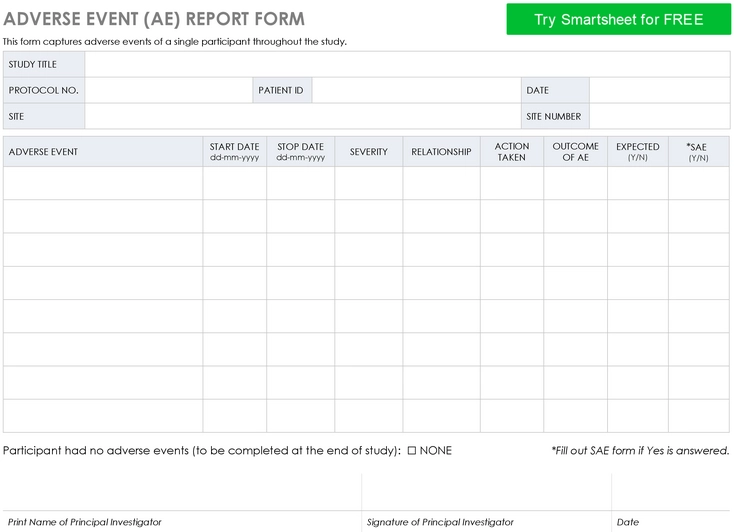
Die Adverse Event (AE) Report Form PDF ist ein wesentlicher Bestandteil der medizinischen Forschung. Sie wurde entwickelt, um adverse Ereignisse von Teilnehmern während einer Studie festzuhalten. Diese Vorlage sorgt dafür, dass alle relevanten Informationen strukturiert und nachvollziehbar dokumentiert werden. Sie unterstützt nicht nur Forscher, sondern auch Institutionen dabei, die Sicherheit und das Wohlbefinden der Studienteilnehmer zu gewährleisten.
Wichtige Aspekte der Vorlage
Die Vorlage enthält mehrere wichtige Felder, die es ermöglichen, ein umfassendes Bild der unerwünschten Ereignisse zu erhalten. Zu den Hauptkomponenten gehören:
- Studientitel und Protokollnummer: Hier werden grundlegende Informationen zur Studie gesammelt.
- Patienten-ID: Ein wichtiger Aspekt zur Identifikation und Nachverfolgbarkeit der Teilnehmer.
- Adverse Event Details: Für jedes unerwünschte Ereignis sind Start- und Enddatum, Schweregrad und Beziehung zur Behandlung zu dokumentieren.
- Maßnahmen: Welche Schritte wurden unternommen? Wurde eine medizinische Intervention erforderlich?
- Ergebnis: Wie hat sich das unerwünschte Ereignis entwickelt? Dies könnte von „gelöst“ bis „Tod“ reichen.
Praktische Anwendungen
Die Verwendung dieser Vorlage ist in verschiedenen Situationen unerlässlich. Sie hilft nicht nur bei der Einhaltung von Vorschriften, sondern auch bei der Analyse von Sicherheitsdaten. Wenn beispielsweise während einer klinischen Studie ein unerwartetes Ereignis auftritt, kann diese Vorlage schnell und effizient genutzt werden, um alle notwendigen Informationen zu erfassen. Die strukturierte Form erleichtert die spätere Auswertung und Berichterstattung erheblich.
Außerdem ist die Vorlage für Studienleiter, Prüfer und medizinisches Personal gedacht, die die Verantwortung für das Wohlergehen der Teilnehmer tragen. Sie ermöglicht eine schnelle und präzise Dokumentation, was in kritischen Situationen entscheidend sein kann.
Empfehlungen für die Nutzung
Um die Vorlage optimal zu nutzen, ist es ratsam, sie regelmäßig zu aktualisieren und an die spezifischen Anforderungen der jeweiligen Studie anzupassen. Eine klare Kommunikation innerhalb des Forschungsteams über die Bedeutung der Dokumentation kann ebenfalls dazu beitragen, die Qualität der gesammelten Daten zu verbessern.
Insgesamt ist die Adverse Event Report Form PDF nicht nur ein nützliches Werkzeug, sondern ein unverzichtbarer Bestandteil jeder klinischen Studie. Sie fördert Transparenz und Sicherheit und trägt zur Verbesserung der Forschung bei.